肝脏是脊椎动物消化系统中的一个器官,以代谢功能为主,并扮演着去毒素、氧化、肝糖原储存、合成分泌性蛋白等重要角色。肝脏直接或间接地参与多个重要代谢途径,与多种遗传性疾病有关,目前已有几百种与肝脏相关的单基因疾病的报道。因此,越来越多的科学家聚焦于借助先进技术展开对靶向肝脏的基因治疗。
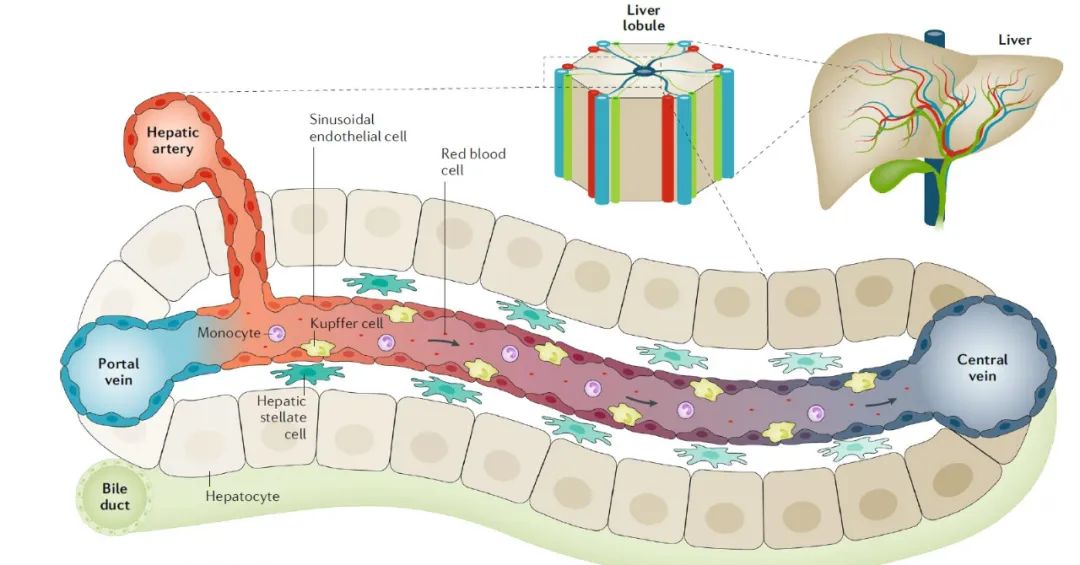
图1 肝脏结构(PMID: 32483353)
得益于病毒载体的发展,借助病毒载体进行靶向肝脏的基因水平或细胞水平操作已成为科学家研究热点。
重组腺相关病毒载体(recombinant Adeno-associated virus, rAAV)和腺病毒载体(Adenovirus)均能高效感染肝脏组织。其中腺病毒的强嗜肝性特点使其被广泛用于肝脏的研究中,相较于其他病毒载体,腺病毒载体具有容量大、快速表达、高效转导等优势,但腺病毒免疫原性强,感染剧烈,故常会引起动物局部组织炎症反应和机体免疫反应,对动物体征和实验结果的客观性造成影响。
rAAV载体是表达基因序列的理想载体,具有血清型种类多样、免疫原性低、长期稳定表达基因、宿主范围广等优势,在基因功能研究和基因治疗递送载体中占据主导地位。
01 rAAV载体血清型的选择
AAV2是第一个被报道用于体内基因递送的载体,其可以有效转导肝细胞。随后,一些常用血清型(AAV8、AAV9、AAV5、AAV3、AAV-DJ)及AAVhu.37、AAVrh.8等AAV血清型载体被发现可以高效转导小鼠肝脏,其中AAV8血清型在小鼠肝脏的转导效率更高(有报道称通过静脉注射对肝脏的转导率为90%以上),且在肝脏中表达时间更长,此外,scAAV8可实现快速、高效、稳定、安全表达的目的。另有研究者发现,AAV8血清型体外转导人肝细胞效果较差。研究者可根据实验目的、实验设计去选择合适的病毒载体。

图2 不同AAV血清型对肝脏转导率比较(PMID: 19861950)
感染效果图

图3 和元生物测试AAV8血清型静脉注射感染肝脏结果
和元生物可提供AAV1-9、AAV-DJ、AAVrh10等几十种AAV血清型病毒包装服务。
02 启动子选择
肝脏中细胞类型主要分为两类:实质细胞(parenchymal cells)和非实质细胞(nonparenchymal cells),其中,实质细胞约占肝脏体积的70-80%。肝细胞(Hepatocyte)是肝脏中最主要的实质细胞,是肝脏基本功能单位—肝小叶的细胞构成,也是肝脏功能的主要承担者,具有调节代谢、解毒的作用,参与蛋白质合成及储存、碳水化合物转换、胆汁的合成与分泌。因此开发高效、特异靶向肝细胞的工具尤为重要。目前,较为常用的肝细胞特异性启动子为:TBG和Alb。此外,在肝脏组成中,还包含肝星状细胞(Hepatic stellate cells, HSCs,也叫Ito细胞)、Kupffer细胞( Kupffer cell, KC)和肝窦内皮细胞(liver sinusoidal endothelial cells,LSECs)等。
表一 常用肝细胞特异性启动子
| 启动子 | 细胞特异性 | |
| TBG | 甲状腺素结合球蛋白 (Thyroxin Binding Globulin) |
肝细胞 |
| Alb | 白蛋白(Albumin) | 成年动物肝细胞(在发育中肝前体细胞中也有会表达) |
| CBh/CAG/CMV等 | 广泛感染 | |
感染效果图
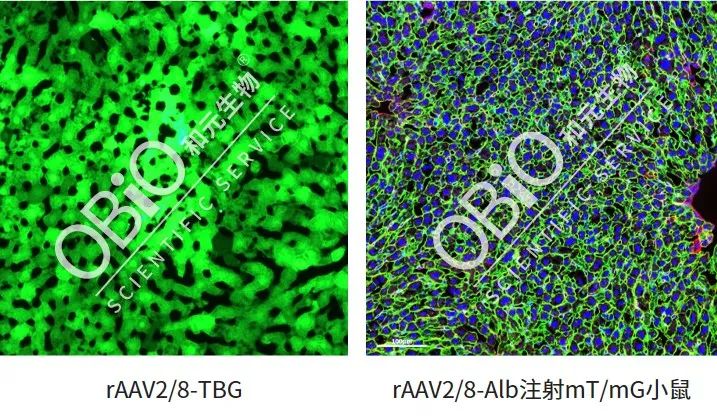
图4 和元生物测试TBG和Alb启动子尾静脉注射感染肝细胞结果
和元生物可提供CBh、CAG、CMV、EF1a等广泛表达启动子,亦可提供靶向肝细胞的TBG和Alb特异性启动子,帮助您构建高效、特异性靶向肝脏的rAAV载体。
03 注射方式及注射剂量
进入肝脏的血管有肝动脉和门静脉。肝动脉发自腹腔动脉干输送富含氧气的血液;门静脉引消化道(肠胃、胰腺、脾脏)的静脉血,输送富含消化营养的血液。出肝脏的血液通过肝静脉,汇入后腔静脉。
基于肝脏的结构特点,靶向肝脏的rAAV载体递送方式主要分为直接注射和系统注射。
表二 靶向肝脏的rAAV载体递送方式
| 方法 | 优势 | 不足 | rAAV用量 | |
| 直接注射 | 肝叶直接注射 (direct injection into the liver lobes) |
高效转导、靶向性强 | 侵入性强、对操作有要求、手术风险大、对动物有伤害。 | — |
| 门静脉注射 (Portal vein injection, PV) |
1E+11vg | |||
| 脾被膜注射 (splenic capsule injection) |
— | |||
| 肝动脉注射 (Hepatic artery, HA) |
— | |||
| 系统注射 | 静脉注射 (intravenous, IV):尾静脉注射和眶后静脉窦注射等 |
操作简单 | 靶向性较直接注射差,可借助肝脏特异性启动子实现静脉注射特异性感染肝脏。 | 1-2E+11vg |
| 腹腔注射 (intraperitoneal, IP) |
约3E+11vg | |||
-
表中注射用量为:成年小鼠注射剂量。
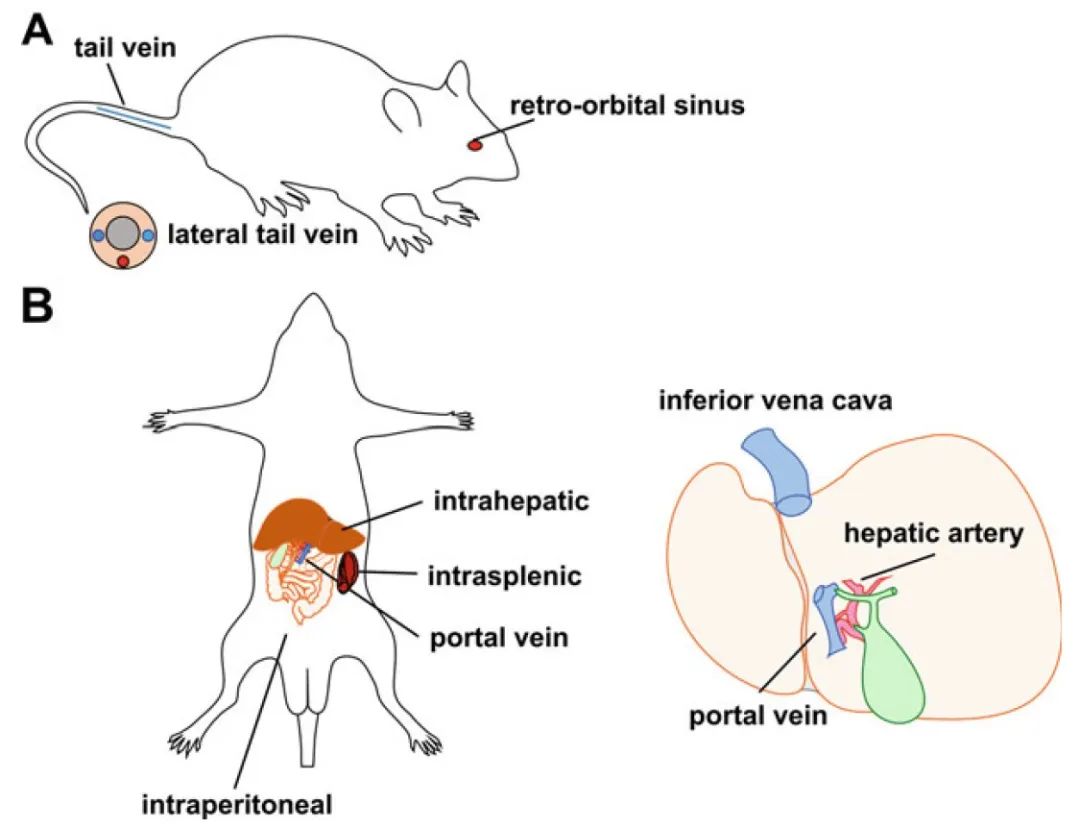
图5 靶向肝脏注射方式(PMID: 30783984)
注射操作视频请点击文末阅读原文
04 应用案例
-
借助rAAV2/8载体携带TBG启动子通过尾静脉注射可特异性感染肝脏,实现对肝脏疾病的机制研究。
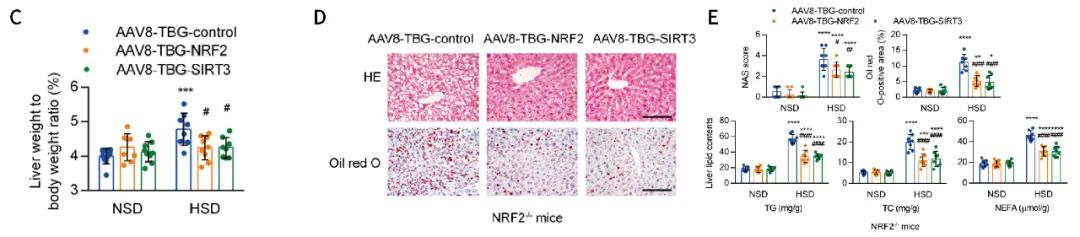
图6 AAV8-TBG感染肝脏(PMID: 35100024)
| 病毒产品 | AAV8-TBG-SIRT3, AAV8-TBG-NRF2 |
| 实验动物 | NRF2−/−小鼠 |
| 注射方式 | 尾静脉注射 |
| 感染部位 | 肝脏 |
| 病毒用量 | 100 μL,2E+11VG |
-
借助rAAV2/8载体进行肝脏的基因水平调控,在肝骨营养不良(HOD)的发病机制中发现了一个新的肝-骨轴,涉及肝脏PP2Acα的上调,导致肝因子卵磷脂-胆固醇酰基转移酶(LCAT)的表达减少,以及胆固醇从骨到肝脏的逆向转运缺陷。(详情请点击【Cell Metab.】肝-骨轴缺陷促进肝性骨营养不良疾病的进展)
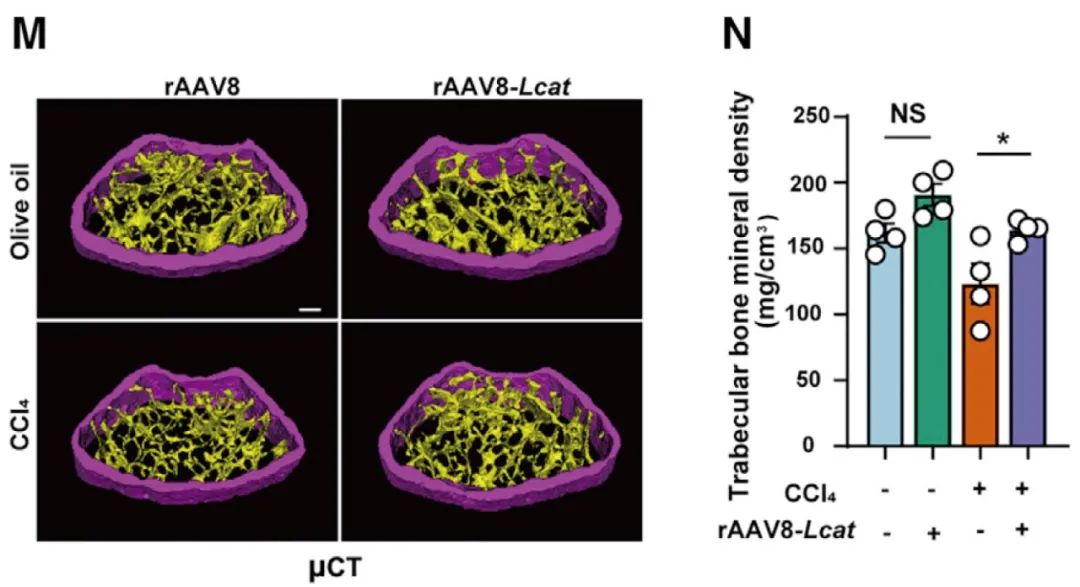
图7 AAV8感染肝脏(PMID: 35235775)
| 病毒产品 | AAV8-Lcat,AAV8-Lcat shRNA |
| 实验动物 | HOD鼠 |
| 注射方式 | 尾静脉注射 |
| 感染部位 | 肝脏 |
| 病毒用量 | 2E+11VG |
参考文献
[1] Nat Rev Gastroenterol Hepatol. 2020 Aug;17(8):457-472. DOI: 10.1038/s41575-020-0304-x
[2] Mol Ther. 2010 Jan;18(1):118-25. DOI: 10.1038/mt.2009.246
[3] Methods Mol Biol. 2019;1950:333-360. DOI: 10.1007/978-1-4939-9139-6_20
[4] Methods Mol Biol. 2011;807:141-57. DOI: 10.1007/978-1-61779-370-7_6
[5] Genes (Basel). 2020 Aug 10;11(8):915. DOI: 10.3390/genes11080915
[6] Expert Opin Biol Ther. 2021 Jun;21(6):749-766. DOI: 10.1080/14712598.2021.1865303
[7] Circulation . 2022 Feb;145(5):375-391. DOI: 10.1161/CIRCULATIONAHA.121.055600
[8] Cell Metab. 2022 Mar 1;34(3):441-457.e7. DOI: 10.1016/j.cmet.2022.02.006
